医歯薬学
2026.02.26
新たな視点:加齢に伴う血液の変化「クローン性造血」が大動脈瘤を悪化させる仕組みを解明~免疫細胞に着目した治療戦略の可能性~
・加齢に伴って生じるクローン性造血*1が、大動脈瘤(りゅう)の拡大を促進することを明らかにした。
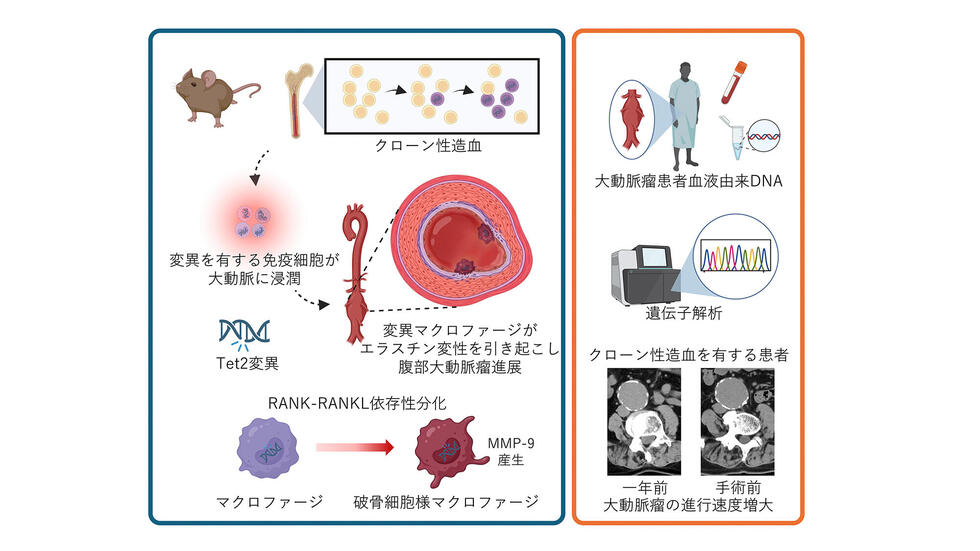
・大動脈瘤悪化の機序として、クローン性造血の原因遺伝子の一つであるTet2*2に変異を有するマクロファージ*3が破骨細胞*4様細胞へと分化し、血管壁の弾力を保つエラスチン*5を分解することで大動脈瘤を増悪させることを見出した。
・この過程に関与するRANK-RANKLシグナル*6を、遺伝学的手法または阻害剤により抑制することで、動物モデルにおける動脈瘤進行が抑制され、大動脈瘤に対する内科的治療戦略の可能性が示された。
名古屋大学大学院医学系研究科循環器内科学の米川淳 大学院生(筆頭著者)、同大学医学部附属病院循環器内科の由良義充 病院助教(同大学高等研究院兼務)(責任著者)、竹藤幹人 講師、同大学大学院医学系研究科循環器内科学の室原豊明 教授と血管外科学の坂野比呂志 教授らの共同研究により、腹部大動脈瘤に対する内科的治療法の開発を目指し、近年「加齢に伴う血液の変化」として注目されているクローン性造血に着目した研究を行いました。
腹部大動脈瘤は、大動脈がこぶ状に拡張する病気で、破裂すると突然死に至ることもある重篤な疾患です。現在、有効な薬物治療はなく、一定以上に拡大した場合には手術(開腹手術やステントグラフト治療)が主な治療法となっています。そのため、動脈瘤の進行を抑える内科的治療の開発が強く求められています。
近年、加齢に伴って血液をつくる細胞に遺伝子変異が生じ、変異を持った特定の血液細胞が増える現象であるクローン性造血が、心血管疾患の新たな危険因子として注目されています。本研究では、このクローン性造血が腹部大動脈瘤の進行にどのように関与しているかを検討しました。
腹部大動脈瘤の手術予定患者の血液由来DNAを解析した結果、クローン性造血を有する患者では、動脈瘤の拡大速度がより速いことが示されました。さらに動物実験により、クローン性造血の原因遺伝子の一つであるTet2に変異を持つ免疫細胞(マクロファージ)が、骨を分解する細胞(破骨細胞)に似た性質を獲得し、血管壁の弾力を保つエラスチンを分解することで、動脈瘤を悪化させる新たな病態メカニズムを解明しました。
また、この過程に関与するRANK-RANKLシグナルを遺伝学的または薬理学的に抑制することで、動物モデルにおける動脈瘤の進行が抑えられることを示しました。
本研究は、腹部大動脈瘤において、血管そのものの要因に加え、血液の加齢性変化という新たな視点から病態を捉え、内科的治療戦略の開発につながることが期待されます。
本研究成果は、2026年2月25日付(日本時間2月26日)、American Society for Clinical Investigation (ASCI) が発行する雑誌『Journal of Clinical Investigation』に掲載されました。
◆詳細(プレスリリース本文)はこちら
◆詳細(プレスリリース英文)はこちら
*1)クローン性造血:加齢に伴って血液をつくる幹細胞に遺伝子変異が生じ、変異をもつ血液細胞が増える現象。心血管疾患などの加齢性疾患との関連が注目されている。
*2)Tet2:血液細胞の分化や機能を調節する遺伝子の一つ。Tet2に変異が生じると、クローン性造血が起こりやすくなることが知られている。
*3)マクロファージ:体内に侵入した異物や傷んだ細胞を処理する免疫細胞。炎症反応の制御に重要な役割を果たすが、過剰に活性化すると組織障害を引き起こすことがある。
*4)破骨細胞:骨を分解する働きを持つ細胞。通常は骨の代謝に関与するが、本研究ではマクロファージが破骨細胞に似た性質を獲得することが示された。
*5)エラスチン:血管の壁に含まれる弾性力を保つためのタンパク質。エラスチンが分解されると血管のしなやかさが失われ、動脈瘤の進行につながる。
*6)RANK-RANKLシグナル:破骨細胞の分化や活性化を制御する重要なシグナル経路。骨代謝だけでなく、炎症や血管病変への関与も注目されている。
雑誌名:Journal of Clinical Investigation
論文タイトル:Tet2-driven Clonal Hematopoiesis Drives Aortic Aneurysm via Macrophage-to-Osteoclast-like Differentiation
著者:Jun Yonekawa1, Yoshimitsu Yura1*, Junmiao Luo1, Katsuhiro Kato1, Shuta Ikeda2, Yohei Kawai2,3, Tomoki Hattori1, Ryotaro Okamoto1, Mari Kizuki1, Emiri Miura-Yura4, Keita Horitani5, Kyung-Duk Min6, Takuo Emoto7, Hiroshi Banno2, Mikito Takefuji1, Kenneth Walsh8, Toyoaki Murohara1
1. Department of Cardiology, Nagoya University Graduate School of Medicine, Nagoya, Japan
2. Division of Vascular and Endovascular Surgery, Department of Surgery, Nagoya University Hospital, Nagoya, Japan
3. Department of Vascular Surgery, Aichi Medical University, Nagakute, Japan.
4. Division of Diabetes, Department of Internal Medicine, Aichi Medical University School of Medicine, Nagakute, Japan.
5. Department of Medicine II, Kansai Medical University, Osaka, Japan
6. Department of Cardiovascular and Renal Medicine, Hyogo Medical University, Hyogo, Japan.
7. Division of Cardiovascular Medicine, Department of Internal Medicine, Kobe University Graduate School of Medicine, Kobe, Japan
8. Division of Cardiovascular Medicine, Robert M. Berne Cardiovascular Research Center, University of Virginia School of Medicine, Charlottesville, VA, United States
DOI: 10.1172/JCI198708
URL: https://doi.org/10.1172/JCI198708
医学部附属病院循環器内科 由良 義充 病院助教
https://www.med.nagoya-u.ac.jp/medical_J/laboratory/clinical-med/internal-med/cardiology/