医歯薬学
2022.03.24
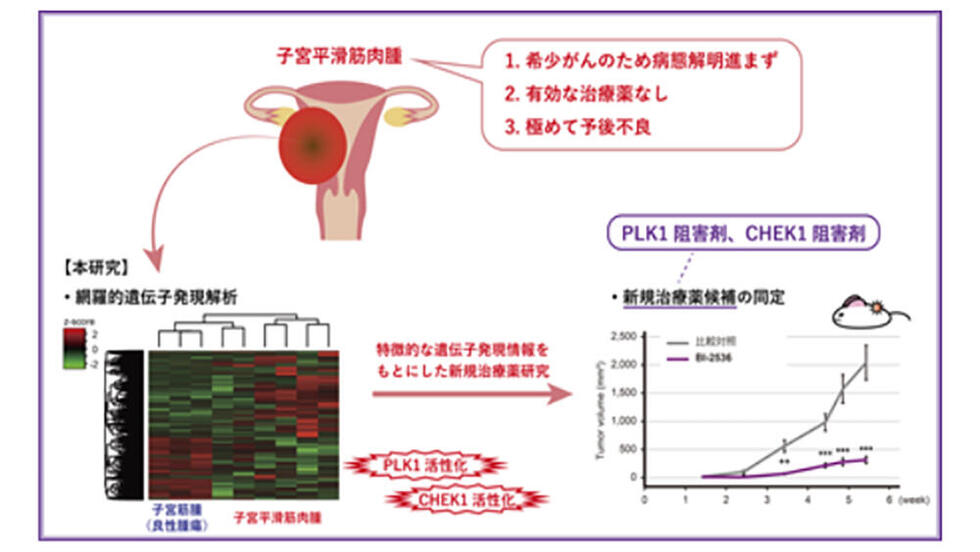
子宮平滑筋肉腫の特徴として、細胞周期関連酵素の異常な活性化の同定 ―新規治療薬として PLK1 および CHEK1 阻害剤の効果が期待―
名古屋大学大学院医学系研究科産婦人科学の梶山広明教授、吉田康将特任助教、同大学医学部附属病院産婦人科の横井暁病院助教、および国立がん研究センター研究所病態情報学ユニットの山本雄介ユニット長、国立がん研究センター中央病院婦人腫瘍科の加藤友康科長らの研究グループは、子宮平滑筋肉腫に対する網羅的な遺伝子発現解析を通して、新たな治療標的として PLK1 遺伝子とCHEK1 遺伝子を同定しました。また、PLK1 阻害剤と CHEK1 阻害剤の抗腫瘍効果を実験的に明らかにしており、これらの薬剤は、子宮平滑筋肉腫に対する新規治療薬として期待されます。
子宮平滑筋肉腫は、いわゆる「不治の病」であり、手術を行ったとしても早期に再発を来し、再発腫瘍に対しては、有効な治療方法はありません。従って、進行・再発平滑筋肉腫患者の予後は、1-2 年と考えられています。また、子宮平滑筋肉腫は、希少がんであるため、その病態に関する基礎研究はあまり進んでいません。本研究においては、子宮平滑筋肉腫の患者組織を使用し、次世代シーケンス* 1 により網羅的に遺伝子発現解析を行いました。その結果、子宮平滑筋肉腫においては、良性腫瘍と比較すると、発現変動している遺伝子が 512 個見つかりました。その 512 個の遺伝子の機能を解析すると、子宮平滑筋肉腫においては、細胞周期* 2 に関わる複数の酵素* 3 が活性化している、すなわち、細胞増殖が異常に速いことが示唆されました。そこで、子宮平滑筋肉腫の細胞株に対して、それらの酵素に対する複数の阻害剤の抗腫瘍効果を試したところ、PLK1 と CHEK1 に対する阻害剤が極めて高い抗腫瘍効果を有することが明らかになりました。さらに、PLK1 阻害剤(BI-2536)と CHEK1 阻害剤(プレクサセルチブ)は、マウスモデルにおいても高い抗腫瘍効果を示しました。PLK1 と CHEK1 阻害剤は、他のがん種においては、臨床試験中の薬剤であり、ヒトに対する安全性は確認されています。従って、子宮平滑筋肉腫に対する新規治療薬として、PLK1 阻害剤と CHEK1 阻害剤は有望であり、臨床試験によりその効果が検証されることが望まれます。
本研究成果は、学術雑誌「Clinical Cancer Research」の電子版(2022 年 3 月 18 日)に掲載されました。
○ 不治の病である子宮平滑筋肉腫に効果が期待される新規治療薬候補が同定された。
○ 網羅的な遺伝子発現の解析により、子宮平滑筋肉腫の病態の一端が明らかにされた。
◆詳細(プレスリリース本文)はこちら
*1 次世代シーケンス:DNA や RNA を解析する装置。2000 年代半ばに登場し、従来の方法より格段に高速に、膨大な量を、安価に解析できるようになりました。
*2 細胞周期:細胞分裂により生じた細胞が、再び分裂して二つの新しい細胞になるまでの過程。細胞周期が速いと、細胞の増殖速度が速いということになります。
*3 酵素:生体内で生じる化学反応を促進するタンパク質。様々な酵素が協調して働くことにより、生命反応は維持されています。
掲雑誌名:Clinical Cancer Research
論文タイトル:Aberrant activation of cell cycle-relate d kinases and the potential therapeutic impact of PLK1 or CHEK1 inhibition in uterine leiomyosarcoma
著者:
Kosuke Yoshida 1,2,3, Akira Yokoi 1,2, Tomofumi Yamamoto 3, Yusuke Hayashi 3, Jun Nakayama 3, Tsuyoshi Yokoi 4, Hiroshi Yoshida 5, Tomoyasu Kato 6, Hiroaki Kajiyama 1, Yusuke Yamamoto 3
所属:
1 Department of Obstetrics and Gynecology, Nagoya University Graduate School of Medicine, Nagoya, Japan
2 Institute for Advanced Research, Nagoya University, Nagoya, Japan
3 Laboratory of Integrative Oncology, National Cancer Center Research Institute, Tokyo, Japan
4 Department of Drug Safety Sciences, Division of Clinical Pharmacology, Nagoya University Graduate School of Medicine, Nagoya, Japan
5 Department of Diagnostic Pathology, National Cancer Center Hospital, Tokyo, Japan
6 Department of Gynecology, National Cancer Center Hospital, Tokyo, Japan
DOI:10.1158/1078-0432.CCR-22-0100
English ver.
https://www.med.nagoya-u.ac.jp/medical_E/research/pdf/Cli_220322en.pdf
大学院医学系研究科 梶山 広明 教授
https://www.med.nagoya-u.ac.jp/obgy/index.html